Sinopharm (Pekino): BBIBP-CorV
FASO 1
1 Provo
ChiCTR2000032459
Ĉinio
FASO 2
2 Provoj
NCT04962906
Argentino
ChiCTR2000032459
Ĉinio
FASO 3
6 Provoj
NCT04984408
ChiCTR2000034780
Unuiĝintaj Arabaj Emirlandoj
NCT04612972
Peruo
NCT04510207
Barejno, Egiptio, Jordanio, Unuiĝintaj Arabaj Emirlandoj
NCT04560881, BIBP2020003AR
Argentino
NCT04917523
Unuiĝintaj Arabaj Emirlandoj
Aproboj
Listigo de Kriz-Uza OMS 59 Landoj
Angolo 、 Argentino 、 Barejno 、 Bangladeŝo 、 Belorusio 、 Belizo 、 Bolivio (Plurinacia ŝtato de) 、 Brazilo 、 Brunejo Darussalam 、 Kamboĝo 、 Kamerunio 、 Ĉadio 、 Ĉinio 、 Komoroj 、 Egiptio 、 Ekvatora Gvineo 、 Gabono 、 Gambio 、 Kartvelio 、 Gujano 、 Hungario 、 ndonesoj 、 Irano (Islama Respubliko) 、 Irako 、 Jordanio 、 Kirgizio 、 Laa Popola Demokratia Respubliko
Libano 、 Malajzio 、 Maldivoj 、 Maŭritanio 、 Aŭricicio 、 Mongolio 、 Montenegro 、 Maroko 、 Mozambiko 、 Namibio 、 Nepalo 、 Niĝero 、 Makedonio Norda 、 Pakistano 、 Paragvajo 、 Peruo 、 Filipinoj 、 Kongo Respubliko 、 enegal 、 Serbio 、 Sejŝeloj 、 Siera-Leono 、 Salomono Insuloj 、 Somalio 、 Srilanko 、 Tajlando 、 Trinidado kaj Tobago 、 Tunizio 、 Unuiĝintaj Arabaj Emirlandoj 、 Venezuelo (Bolivariana Respubliko) 、 Vjetnamio 、 Zimbabvo
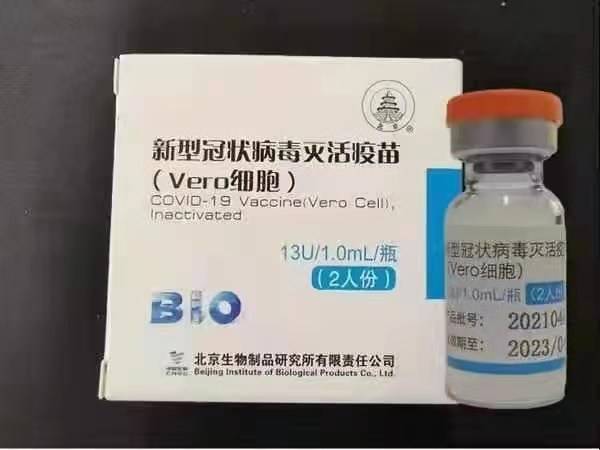
Sinopharm BBIBP-CorV COVID-19 estas inaktivigita vakcino farita el kultur-kreskitaj virusaj eroj, al kiuj mankas patogena kapablo. Ĉi tiu vakcina kandidato estis disvolvita de Sinopharm Holdings kaj la Pekina Instituto pri Biologiaj Produktoj.
La vakcino Sinopharm BBIBP-CorV funkcias permesante al la imunsistemo produkti antikorpojn kontraŭ SARS-CoV-2 beta-koronaviruso. Malaktivigitaj virusaj vakcinoj estas uzataj de jardekoj, kiel kontraŭ rabia vakcino kaj kontraŭ hepatito. Ĉi tiu disvolva teknologio sukcese aplikiĝis al multaj konataj vakcinoj, kiel ekzemple la rabia vakcino.
La trostreĉo SARS-CoV-2 de Sinopharm (trostreĉo WIV04 kaj biblioteka numero MN996528) estis izolita de paciento en Jinyintan Hospital en Wuhan, Ĉinio. La viruso disvastiĝis en kulturo en kompetenta ĉela linio Vero, kaj la supernatanto de infektitaj ĉeloj estis malaktivigita per β-propiolaktono (1: 4000 vol / vol, 2 ĝis 8 ° C) dum 48 horoj. Post klarigo de ĉelaj ruboj kaj ultrafiltrado, dua β-propiolaktona malaktivigo estis farita sub la samaj kondiĉoj kiel la unua malaktivigo. Laŭ OMS, la vakcino estis adsorbita sur 0,5 mg da aluno kaj ŝarĝita en antaŭplenajn injektilojn en 0,5 ml da sterila fosfat-bufrita salo sen konserviloj.
La 31an de decembro 2020, la Ŝtata Medikamenta Administracio anoncis la aprobon de la eksperimenta vakcino disvolvita de Sinopharm.
La 7-an de majo, 2021, la Monda San-Organizo anoncis la aprobon de la vakcino. La listo de urĝa uzo de OMS ebligis landojn rapidigi siajn proprajn reguligajn aprobojn por importi kaj administri vakcinon COVID-19. La Konsila Fakgrupo de OMS pri Imunigaj Strategioj ankaŭ kompletigis sian revizion pri la vakcino. Surbaze de ĉiuj disponeblaj pruvoj, OMS rekomendas du dozojn da vakcino, apartigitaj de tri al kvar semajnoj, por plenkreskuloj de 18 jaroj kaj pli. Vakcina efikeco kontraŭ simptoma kaj enhospitaligita malsano estas taksita je 79% por ĉiuj aĝoklasoj kune.
La Usona Medicina Asocio publikigis "A Randomized Clinical Trial: Effect of 2 Inactivated SARS-CoV-2 Vaccines on Symptomatic COVID-19 Infection in Adults" la 26an de majo, 2021, konkludante, ke "en ĉi tiu antaŭdifinita provizora analizo de hazarda klinika provo, plenkreskuloj La 2 senaktivigitaj SARS-CoV-2-vakcinoj administritaj en ĉi tiu antaŭdifinita provizora analizo de randomigitaj klinikaj provoj signife reduktis la riskon de simptoma COVID-19, kaj gravaj adversaj eventoj estis maloftaj. " En ĉi tiu fazo 3 hazarda provo en plenkreskuloj, la efikeco de la 2 inaktivigitaj tutvirusaj vakcinoj en simptomaj COVID-19-kazoj estis 72.8% kaj 78.1%, respektive. 2 vakcinoj havis maloftajn gravajn adversajn eventojn kun simila ofteco al la nur-alun-kontrolgrupo, kaj plej multaj ne rilatis al vakcinado. Esplora analizo trovis, ke la 2 vakcinoj induktis mezureblajn neŭtraligajn antikorpojn, simile al la rezultoj de la fazo 1/2-testo.
La Laborgrupo WHO SAGE publikigis recenzon de la vakcino Sinopharm / BBIBP COVID-19 la 10an de majo 2021. La vakcino COVID-19 de GAVI asimilas vakuan fiolon-monitoron, kiu diras al sanaj laboristoj ĉu la vakcino estis konservita ĝuste kaj ne estis elmetita al trovarmiĝo. Rezulte de damaĝo, GAVI raportis la 14-an de majo, 2021. inteligentaj etikedoj fabrikitaj de Zebra Technologies kaj faritaj de Temptime Corporation, konsistas el cirklo kun pli helkolora kvadrato en la mezo, farita el senkolora kemiaĵo, kiu neinversigeble disvolvas koloron laŭlonge de la tempo. . Ĉi tio fariĝas pli malhela por doni vidan indikon pri akumula varma ekspozicio. Post kiam la fiolo estis eksponita al varmeco preter sia optimuma stoka distanco, la kvadrato fariĝas pli malhela ol la cirklo, indikante ke la vakcino ne plu uzu.
Regiona numero de nacia medikamento BBIBP-CorV COVID-19-vakcina medikamenta biblioteko: DB15807.